泛在電力物聯網技術架構全解析與物聯網應用服務
隨著數字化和智能化的發展,泛在電力物聯網已成為推動能源行業轉型的關鍵技術。它通過深度融合物聯網、大數據、云計算和人工智能等技術,構建起一個全面感知、高效協同的電力系統。本文將對泛在電力物聯網的技術架構進行全面解析,并探討其核心應用服務。
一、泛在電力物聯網技術架構
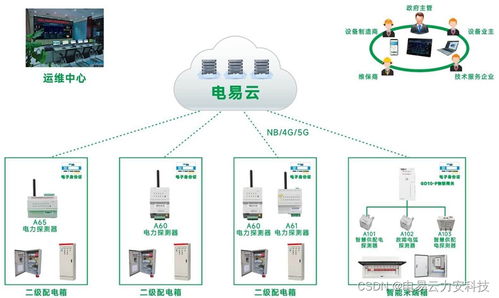
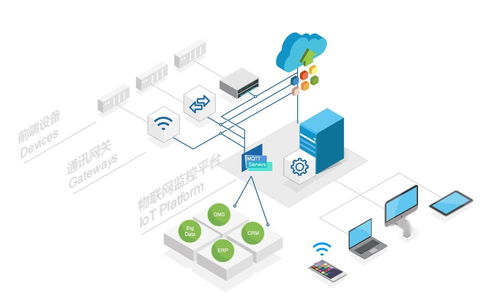
泛在電力物聯網的技術架構通常分為四個層級:感知層、網絡層、平臺層和應用層,每一層都承擔著獨特的角色,共同支撐整個系統的運行。
- 感知層:作為底層基礎,感知層負責采集電力系統中的各類數據。它主要包括智能電表、傳感器、監控設備等硬件,能夠實時監測電壓、電流、功率、設備狀態等信息。這些數據是后續分析和決策的基礎,確保了系統的實時性和準確性。
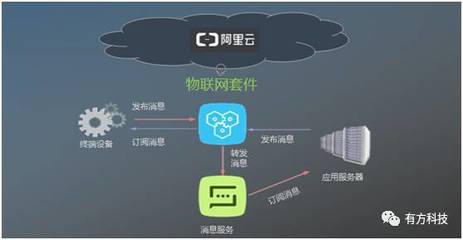
- 網絡層:網絡層負責數據的傳輸和通信,將感知層采集的信息高效、安全地傳送到平臺層。它采用多種通信技術,如5G、光纖、無線局域網(WLAN)和電力線通信(PLC),以適應不同場景的需求。網絡層還包括邊緣計算節點,可對數據進行初步處理,降低延遲并提高響應速度。
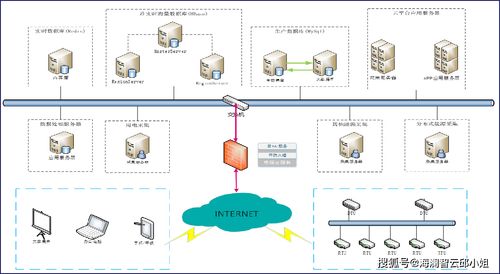
- 平臺層:平臺層是泛在電力物聯網的核心,負責數據的存儲、處理和分析。它通常基于云計算和大數據平臺,整合來自網絡層的數據,并提供數據管理、設備管理、安全認證和智能分析等功能。通過人工智能算法,平臺層能夠實現故障預測、負荷優化和能源調度,提升系統的智能化水平。
- 應用層:應用層面向最終用戶,提供多樣化的服務接口和應用程序。它將平臺層處理后的數據轉化為實際應用,如智能電網監控、需求側管理、分布式能源集成等。應用層還支持與其他系統(如智慧城市平臺)的集成,拓展了物聯網在電力領域的應用范圍。
二、物聯網應用服務
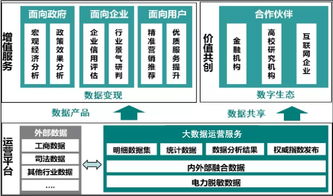
泛在電力物聯網的應用服務廣泛覆蓋電力生產、傳輸、分配和消費各環節,主要體現為以下幾個方面:
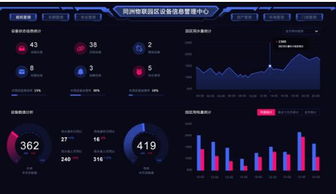
- 智能電網監控與管理:通過實時數據采集和分析,實現對電網狀態的全面監控。例如,系統可自動檢測線路故障、預測設備維護需求,并優化電網運行策略,提高供電可靠性和效率。
- 需求側響應與能源管理:基于用戶用電數據,物聯網技術能夠動態調整負荷,實現削峰填谷。用戶可通過移動應用查看用電情況,參與需求響應計劃,從而降低用電成本并促進能源節約。
- 分布式能源集成:隨著可再生能源(如太陽能、風能)的普及,物聯網技術幫助整合分布式能源資源。它能夠協調發電、儲能和用電,確保電網穩定,并支持微電網的獨立運行。
- 預測性維護與資產管理:利用大數據和AI分析,系統可預測設備故障風險,提前安排維護,減少停機時間。物聯網技術還能優化資產生命周期管理,降低運營成本。
- 用戶服務與互動:通過智能電表和移動平臺,用戶可以獲得個性化用電報告、節能建議和遠程控制功能。這不僅提升了用戶體驗,還促進了能源消費的透明化和智能化。
泛在電力物聯網的技術架構以其多層協同設計,為電力系統提供了強大的支撐。其應用服務不僅提升了電網的智能化和可靠性,還推動了能源行業的可持續發展。隨著技術的不斷演進,泛在電力物聯網將在智慧能源領域發揮更加重要的作用。
如若轉載,請注明出處:http://www.0898znj.cn/product/43.html
更新時間:2026-03-26 02:03:02